Cẩn trọng trong việc sử dụng Molnupiravir trong điều trị Covid 19: cân nhắc giữa lợi ích và nguy cơ về sức khoẻ.
Molnupiravir là một loại thuốc hoạt động dựa trên phương thức đưa các lỗi vào mã di truyền của virus SARS-COV-2, giúp ngăn ngừa virus tái tạo thêm. Thuốc được Cơ quan quản lý thực phẩm và dược phẩm Hoa Kỳ cấp phép sử dụng khẩn cấp trong điều trị COVID-19.
Tổng quan về Molnupiravir
Molnupiravir là một loại thuốc hoạt động dựa trên phương thức đưa các lỗi vào mã di truyền của virus SARS-COV-2, giúp ngăn ngừa virus tái tạo thêm. Thuốc được Cơ quan quản lý thực phẩm và dược phẩm Hoa Kỳ cấp phép sử dụng khẩn cấp trong điều trị COVID-19.
Ngày 23 tháng 12 năm 2021, Cơ quan quản lý thực phẩm và dược phẩm Hoa Kỳ (FDA) đã cấp phép sử dụng khẩn cấp (giấy EUA) cho Merck’s molnupiravir để điều trị bệnh do coronavirus mức độ từ nhẹ đến trung bình (COVID-19) ở người lớn có kết quả dương tính với xét nghiệm virus SARS-COV-2 trực tiếp, và những người có nguy cơ cao tiến triển thành COVID-19 mức độ nghiêm trọng, bao gồm cả nhập viện hoặc tử vong, và các trường hợp mà các lựa chọn điều trị COVID-19 thay thế khác (được FDA cấp phép) không thể tiếp cận hoặc không phù hợp về mặt lâm sàng. Thuốc chỉ được bán khi được bác sĩ kê đơn, và phải được điều trị càng sớm càng tốt sau khi xác định mắc COVID-19, cũng như sử dụng trong vòng 5 ngày kể từ khi bắt đầu có triệu chứng.
FDA cũng tuyên bố thuốc không được phép sử dụng cho người mắc COVID-19 dưới 18 tuổi vì thuốc có thể ảnh hưởng đến sự phát triển của xương và sụn. Thuốc cũng không được phép sử dụng trong việc phòng ngừa trước hoặc sau phơi nhiễm với COVID-19, hoặc bắt đầu điều trị ở bệnh nhân đã nhập viện do COVID-19 vì chưa quan sát thấy những lợi ích của việc sử dụng thuốc ở các nhóm đối tượng này.
Cơ chế của Molnupiravir
Molnupiravir (Viện phát triển thuốc Emory-2801 [EIDD-2801] / MK-4482) là một trong những loại thuốc uống được phát triển bởi Viện phát triển thuốc - trường đại học Emorry, Atlanta - Hoa Kỳ, sau đó được Ridgeback therapeutics hợp tác cùng Merck & Co mua lại.
Molnupiravir có cơ chế hoạt động nhắm vào enzyme RNA phụ thuộc RNA-polymerase (RdRp) mà virus sử dụng để để phiên mã và sao chép bộ mã RNA. Molnupiravir có cơ chế hoạt động khác một chút với Remdesivir. Đối với Remdesivir, thuốc ngăn cản RdRp và do đó làm virus mất khả năng sao chép, trong khi Molnupiravir có cơ chế hoạt động độc đáo hơn và khá giống với Favipiravir.
Bản chất Molnupiravir là tiền chất ribonucleoside phân tử nhỏ của N-hydroxycytidine (NHC), có hoạt tính chống lại virus SARS-COV-2 và các virus bản chất RNA khác. Sau khi uống Molnupiravir, NHC tham gia vào hệ thống tuần hoàn và được phosphoryl hóa thành NHC triphosphat. NHC triphosphat được kết hợp vào RNA virus bởi RNA-polymerase của virus và điều chỉnh gây polymerase gây sai lệch trong việc kết hợp guanosine hoặc adenosine trong quá trình sao chép. Điều này dẫn đến tích tụ dần các lỗi trong sao chép, tạo thành một hệ thống lỗi nghiêm trọng trong toàn bộ gen, cuối cùng khiến virus không thể lây nhiễm và tái tạo.
Quá trình phát sinh đột biến bao gồm 2 bước, được tóm tắt bởi sơ đồ dưới:
- Bước 1: RdRp tổng hợp bộ gen sợi âm (-gRNA) bằng cách sử dụng bộ gen sợi dương (+gRNA) làm khuôn mẫu.
- Bước 2: +gRNA hoiawjc RNA bộ gen phụ được tổng hợp bằng cách sử dụng RNA chứa M làm khuôn mẫu. RNA chứa M trong -gRNA gây ra đột biến trong +gRNA và RNA bộ gen phụ sau đó được hình thành dẫn dẫn đến đột biến gây chết cho virus
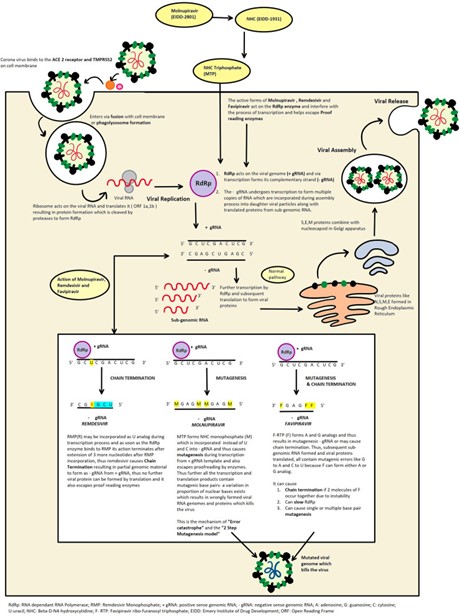
Hình ảnh: So sánh sự khác nhau trong cơ chế hoạt động của các loại thuốc. (Molnupiravir chống lại virus SARS-COV-2 bằng cách gây ra các đột biến trong RNA, trong khi Remdesivir hoạt động bằng cách làm ngưng trệ RdRp lần lượt và gây ra kết thúc chuỗi sợi RNA mới hình thành, và Favipiravir hoạt động bằng cách làm chậm/ngưng trệ RdRp gây ra sự kết thúc chuỗi mới/hoặc gây đột biến/hoặc cả 2 cách)
Molnupiravir đã được đánh giá trong một số thử nghiệm giai đoạn 1 và 2. Trên cơ sở phân tích từ các thử nghiệm giai đoạn 2, liều 800mg được lựa chọn để nghiên cứu thêm, bao gồm cả các đánh giá trong giai đoạn 3 thử nghiệm trên người trưởng thành có nguy cơ, không nhập viện, có dấu hiệu khởi phát hoặc triệu chứng COVID-19 đã xảy ra không quá 5 ngày trước đó.
Nghiên cứu trong điều trị COVID-19: hiệu quả và tác dụng phụ
Nghiên cứu giai đoạn 1
Thử nghiệm giai đoạn 1 mù đôi, ngẫu nhiên có đối chứng đầu tiên (NCT04392219) trên 130 người tình nguyện khỏe mạnh cho thấy Molnupiravir có khả năng dung nạp tốt, dược động học tương ứng với liều khi sử dụng. Sau khi uống thuốc, tiền thuốc Molnupiravir được phân cắt nhanh chóng thành dạng hoạt động EIDD-1931 với thời gian trung bình là 1-1,75 giờ. Thời gian bán thải thuốc kéo dài 1 giờ với giai đoạn thải trừ chậm hơn rõ ràng sau khi dùng đơn liều cao hoặc nhiều liều, nhưng không có sự tích lũy được ghi nhận khi dùng nhiều lần.
Liều dao động trong khoảng 50–800 mg dùng hai lần mỗi ngày trong 5,5 ngày và một liều duy nhất lên đến 1600 mg được cho là an toàn và dung nạp tốt. Đối với khả năng dung nạp, một tỷ lệ lớn bệnh nhân trong nhóm chứng (sử dụng giả dược) gặp phải tác dụng phụ cao hơn so với nhóm sử dụng thuốc ở cả liều đơn (43,8% so với 35,4) và nhiều liều tăng dần (50,0% so với 42,9%). Trong khi nhức đầu là tác dụng phụ được báo cáo thường xuyên nhất trong liều tăng dần đơn lẻ (nhóm chứng có tỷ lệ đau đầu cao hơn so với nhóm sử dụng thuốc, tương ứng 18,8% so với 12,5%), tiêu chảy là tác dụng phụ được báo cáo thường xuyên nhất được ghi nhận (7,1% mỗi nhóm). Không thấy bất thường có ý nghĩa lâm sàng, hoặc các dấu hiệu sinh tồn hay điện tâm đồ, cũng như bất kỳ tác dụng phụ nghiêm trọng được ghi nhận. Chỉ có một đối tượng bị ngưng thuốc vì phát ban sẩn ngứa nhẹ sau khi dùng liều lượng 800 mg hai lần mỗi ngày được cho rằng có liên quan đến thuốc.
Một thử nghiệm giai đoạn Ib/IIa ngẫu nhiên có đối chứng trên nhãn mở (với 18 đối tượng tham gia) được triển khai tại Cơ sở Nghiên cứu Lâm sàng Hoàng gia Liverpool và Broadgreen bằng cách sử dụng phương pháp Bayes. Bệnh nhân người lớn với RT-PCR xác nhận nhiễm SARS-CoV-2 trong vòng 5 ngày kể từ khi khởi phát triệu chứng được đưa vào và chọn ngẫu nhiên vào một trong các tiêu chuẩn: hoặc 300, 600 và 800 mg liều Molnupiravir, 02 lần mỗi ngày trong 5 ngày bằng đường uống. Mục tiêu chính của nghiên cứu là đánh giá độc tính giới hạn liều trong khi các mục tiêu thứ cấp bao gồm đánh giá mức độ an toàn và tiến triển lâm sàng. Tiêu chuẩn đặt ra là một liều được coi là không an toàn hoặc độc hại ở mức không thể chấp nhận được nếu xác suất của độc tính giới hạn là 30% hoặc lớn hơn so với các đối chứng. Kết quả cho thấy, tất cả bệnh nhân dùng các mức hàm lượng được phát hiện có các tác dụng phụ nhẹ. Điều này cho thấy liều cao nhất 800mg x 2 lần/ngày có xác suất 0,9% gây độc tính, và do đó Molnupiravir trước mắt được coi là an toàn và dung nạp tốt.
Nghiên cứu giai đoạn 2
Một thử nghiệm mù đôi, ngẫu nhiên có đối chứng, đa trung tâm, pha IIa (MK-4482-006) đã được tiến hành (NCT04405570, n = 202) để đánh giá tính an toàn và khả năng dung nạp ở bệnh nhân COVID-19 mức độ nhẹ đến trung bình. Hai lần mỗi ngày với liều uống 200 mg, 400 mg và 800 mg Molnupiravir trong 5 ngày được sử dụng ở nhóm thử nghiệm so với nhóm chứng sử dụng giả dược, sau khi phân nhóm ngẫu nhiên. Đánh giá thời gian để thanh thải RNA của virus trong tăm bông ngoáy dịch mũi họng (bằng RT-PCR) là mục tiêu chính, trong khi mục tiêu phụ của thử nghiệm bao gồm đánh giá thời gian để loại trừ virus lây nhiễm khỏi bông dịch mũi họng và sự thay đổi RNA trung bình so với ban đầu vào các ngày 3, 5 và 7. Đánh giá hoạt động, độ an toàn và khả năng dung nạp được thực hiện trong 28 ngày sau khi bắt đầu nghiên cứu. Kết quả cho thấy, thời gian để thanh thải (âm tính RNA) đã giảm đáng kể ở nhóm sử dụng thuốc với liều 800 mg x 2 lần mỗi ngày so với nhóm chứng (p = 0,013, trung vị: 14 ngày). Hơn nữa, việc giảm thời gian thanh thải RNA của virus cũng lớn hơn và có ý nghĩa khi so sánh với nhóm chứng (trung bình: 14 ngày so với 27 ngày; giá trị p = 0,01). Việc phân lập virus thấp hơn đáng kể ở những nhóm sử dụng liều 800 mg x 2 lần mỗi ngày so với nhóm chứng (1,9% so với 16,5%, p = 0,02) vào ngày 3. Vào ngày 5, không ghi nhận sự phân lập virus nào từ những bệnh nhân dùng liều 400 hoặc 800mg molnupiravir x 2 lần mỗi ngày so với 11,1% ở nhóm chứng (p = 0,03). Tỷ lệ đối tượng đạt được mức âm tính với SARS-CoV-2 vào cuối nghiên cứu là 92,5%, 78,7%, 91,3% tương ứng với các liều 800mg, 400mg, 200mg và đều sử dụng 2 lần mỗi ngày, trong khi nhóm chứng là 80,3%.
Về khả năng dung nạp, nhìn chung, rất ít các tác dụng phụ mức độ nhẹ được ghi nhận trong nghiên cứu, và thấp nhất ở nhóm sử dụng liều 800mg x 2 lần/ngày. Nhức đầu, mất ngủ và tăng nồng độ alanin aminotransferase (ALT) là các tác dụng phụ được báo cáo ở 4 đối tượng tham gia, và có 5% nhóm sử dụng thuốc so với 8,1% nhóm chứng lần lượt có các tác dụng phụ cấp độ 3. Có 2/140 (1,4%) so với 1/62 (1,6%) tác dụng phụ dẫn đến việc ngừng sử dụng ở nhóm sử dụng thuốc và nhóm chứng tương ứng. Việc bị ngừng điều trị ở 4 bệnh nhân là do các tác dụng phụ nghiêm trọng. Điều này bao gồm một bệnh nhân được nhóm chứng bị thiếu oxy, 2 bệnh nhân từ nhóm sử dụng 400mg bị giảm độ bão hòa oxy và tai biến mạch máu não, và 1 bệnh nhân nhóm sử dụng liều 800mg bị suy hô hấp cấp tính. Một trường hợp tử vong đã được báo cáo ở một bệnh nhân nhóm chứng bị thiếu oxy.
Nghiên cứu giai đoạn 3
Nghiên cứu ngẫu nhiên mù đôi giai đoạn III (MOVe-OUT) được lên kế hoạch để đánh giá hiệu quả và độ an toàn của thuốc ở 1850 người lớn (18 tuổi trở lên) không nhập viện (NCT04575597, MK-4482-002) gần đây đã bị ngừng bởi hội đồng giám sát an toàn dữ liệu độc lập, do lợi ích quá mức trong nhóm điều trị tích cực so với nhóm chứng. Phân tích tạm thời (trên 775 đối tượng) cho thấy nguy cơ nhập viện hoặc tử vong giảm đáng kể tới 50% (p = 0,0012) vào ngày thứ 29. Bên cạnh đó, 7,3% bệnh nhân (28/385) nhóm sử dụng thuốc so với 14,1% bệnh nhân nhóm chứng (53/377) đã nhập viện hoặc tử vong, và không có trường hợp tử vong nào được báo cáo ở nhóm dùng thuốc so với 8 trường hợp tử vong ở nhóm chứng vào ngày thứ 29. Hơn nữa, hiệu quả của thuốc không bị ảnh hưởng bởi biến thể SARS-CoV-2 (gamma, delta hoặc mu), cũng như không bị ảnh hưởng bởi thời điểm khởi phát các triệu chứng và với các yếu tố nguy cơ tiềm ẩn. Tỷ lệ xảy ra bất kỳ tác dụng phụ nào (tương ứng là 35% nhóm sử dụng thuốc so với 40% ở nhóm chứng) và các tác dụng phụ liên quan đến thuốc (12% ở nhóm sử dụng thuốc so với 11% ở nhóm chứng) được phát hiện là tương tự nhau.
Một nghiên cứu ngẫu nhiên mù đôi giai đoạn 3 khác (MOVe-IN, NCT04575584) được lên kế hoạch để đánh giá hiệu quả và độ an toàn của Molnupiravir ở 304 người lớn (18 tuổi trở lên) nhập viện do COVID-19 (MK-4482-001) đã bị chấm dứt sau khi phân tích tạm thời dữ liệu cho thấy nó không có khả năng chứng minh lợi ích lâm sàng ở bệnh nhân nhập viện. Tuy nhiên, một nghiên cứu lớn (trên 1,332 người tham gia) tại pha III (NCT04939428) hiện đang đánh giá hiệu quả và độ an toàn của thuốc trong việc phòng ngừa COVID-19 ở người lớn (MOVe-AHEAD) sống chung với một người có COVID-19, với giả thuyết rằng molnupiravir sẽ vượt trội hơn giả dược trong việc ngăn ngừa nhiễm COVID-19 đã được xác nhận mức độ phòng thí nghiệm cho đến ngày thứ 14.
Hetero Labs Limited, Hyderabad, Ấn Độ đã công bố kết quả tạm thời vào ngày 9 tháng 7 năm 2021, từ thử nghiệm của họ (CTRI/2021/05/033739) trên 741 bệnh nhân COVID-19 mức độ nhẹ. Kết quả tạm thời cho thấy:
- 1) Cải thiện lâm sàng sớm hơn (giảm 2 điểm trong Thang tiến triển lâm sàng của WHO) ở ngày thứ 5 (63,4% so với 22,3%, p <0,0001); ngày 10 (lần lượt là 79,0% so với 49,5%; p <0,0001) và ngày 14 (lần lượt là 81,6% so với 73,2%; p = 0,02)
- 2) Thời gian cải thiện lâm sàng nhanh hơn khi sử dụng thuốc (thời gian trung bình: 8 ngày so với 12 ngày tương ứng; p = 0,0001)
- 3) Âm tính RT-PCR cao hơn (tất cả p <0,0001) ở ngày thứ 5 (tương ứng là 77,4% so với 26,1%), ngày 10 (94,0% so với 57,2%, tương ứng) và ngày 14 (97,0% so với 85,2%)
- 4) Ít nhập viện hơn đáng kể (1,9% so với 6,2%; p = 0,003) trong 14 ngày.
- Không có trường hợp tử vong nào được báo cáo ở cả hai nhóm. Buồn nôn, tiêu chảy và đau đầu là những phản ứng phụ phổ biến nhất được báo cáo - tất cả đều ở mức độ nhẹ. Không có đối tượng ngừng thử nghiệm.
Nói chung, báo cáo tạm thời này cho thấy tỷ lệ nhập viện thấp hơn đáng kể ở những bệnh nhân sử dụng thuốc mắc COVID-19 mức độ nhẹ, và không có tác dụng phụ do thuốc gây ra rõ ràng, mặc dù không có sự khác biệt về tỷ lệ tử vong giữa hai nhóm.
Một báo cáo tạm thời khác từ thử nghiệm giai đoạn 3 của molnupiravir ở bệnh nhân COVID-19 nhẹ từ Ấn Độ đã được Optimus pharma (CTRI / 2021/06/033992) công bố vào ngày 21 tháng 7 năm 2021. Kết quả tạm thời đầu tiên trên 353 bệnh nhân cho thấy RT-PCR âm tính cao hơn ở nhóm sử dụng thuốc so với nhóm chứng (tương ứng là 78,3% so với 48,4%) vào ngày thứ 5. Optimus Pharma cũng ghi nhận sự gia tăng đáng kể mức độ giảm của RT-PCR ở nhóm sử dụng thuốc so với nhóm chứng ngày thứ 5 (77,4% so với 51,5%, p <0,0001) và ngày 10 (99,5% so với 69,5%; p <0,0001), mặc dù không có sự khác biệt nào được ghi nhận ở ngày 14 (99,5% so với 98,5%; p = 0,62) trong một phân tích tạm thời trên 403 bệnh nhân. Cải thiện lâm sàng nhanh hơn (cải thiện ít nhất một điểm so với ban đầu trên thang thứ tự của WHO) cũng được quan sát thấy ở nhóm sử dụng thuốc so với nhóm chứng cả ngày thứ 5 (lần lượt là 79,0% so với 51,3%; p <0,0001) và ngày 10 (97,8% so với 82,3%; p <0,0001). Tuy nhiên, không có sự khác biệt nào được ghi nhận ở ngày thứ 14. Đã có 1 trường hợp nhập viện ở nhóm dùng thuốc so với 3 trường hợp ở nhóm chứng; và 6,5% đối tượng ở nhóm sử dụng thuốc có các tác dụng phụ so với 8,9% ở nhóm chứng. Các tác dụng phụ nghiêm trọng đã được báo cáo ở 1 đối tượng trong nhóm sử dụng thuốc molnupiravir so với 3 đối tượng ở nhóm chứng. Nói chung, báo cáo tạm thời này cũng cho thấy sự phục hồi về mặt lâm sàng và virus (âm tính RT-PCR) nhanh hơn khi sử dụng Molnupiravir so với nhóm chứng, mà không có bất kỳ tác dụng phụ liên quan đến thuốc rõ ràng nào đối với các bệnh nhân mức độ nhẹ. Một số nghiên cứu đang diễn ra khác về Molnupiravir trong COVID-19 mức độ nhẹ cũng được các công ty dược phẩm Ấn Độ khác nghiên cứu.
Các yếu tố nguy cơ và khuyến cáo khi sử dụng Molnupiravir
Hiện tại, liều sử dụng của Molnupiravir được khuyến nghị là 800mg (4 viên x 200mg) uống mỗi 12 giờ trong vòng 5 ngày. Thuốc nên được sử dụng càng sớm càng tốt, sau khi chẩn đoán mắc COVID-19. Không sử dụng thuốc quá 5 ngày.
Theo khuyến cáo, thuốc chỉ được sử dụng cho người trên 18 tuổi. Không sử dụng cho người dưới 18 tuổi do ảnh hưởng của thuốc đến sự phát triển của xương và sụn.
Một số yếu tố nguy cơ và cảnh báo đặc biệt khi sử dụng thuốc bao gồm:
- Suy thận và suy gan. Người suy thận nặng và suy gan đều không được đưa vào thử nghiệm thuốc trên lâm sàng.
- Người tương tác với bất kỳ thành phần nào của thuốc
Thuốc cũng chưa phát hiện các tương tác lâm sàng nào trong thời gian nghiên cứu. Không có rủi ro đáng kể đối với tương tác thuốc khi sử dụng với liều 800mg cứ 12 giờ một lần trong 5 ngày.
Một số yếu tố nguy cơ khác bao gồm:
- Phụ nữ có khả năng sinh sản. Phụ nữ có khả năng sinh sản cần phải sử dụng biện pháp tránh thai hiệu quả trong suốt thời gian điều trị, và 4 ngày sau liều thuốc cuối cùng. Hiện tại chưa có nghiên cứu về độc tính của thuốc trên phụ nữ mang thai. Nghiên cứu về sử dụng thuốc trên động vật đã cho thấy độc tính của thuốc trong thời gian này. Theo đó, sử dụng Molnupiravir trên chuột mang thai trong giai đoạn hình thành các cơ quan dẫn đến khả năng chết phôi thai và gây quái thai cao gấp 7,5 lần so với liều phơi nhiễm khuyến nghị ở người. Nghiên cứu việc sử dụng Molnupiravir trên thỏ mang thai trong giai đoạn hình thành các cơ quan cho thấy việc giảm trọng lượng cơ thể thai nhi gấp 18 lần so với liều phơi nhiễm khuyến nghị ở người. Do vậy thuốc không được khuyến cáo sử dụng trong thời gian mang thai, và phụ nữ trong độ tuổi sinh sản không sử dụng biện pháp tránh thai hiệu quả.
- Bà mẹ cho con bú. Chưa có nghiên cứu về thuốc và bất kỳ thành phần nào của thuốc có trong sữa mẹ, hay ảnh hưởng đến khả năng sản xuất sữa mẹ. Các nghiên cứu về việc tiết sữa trên động vật chưa được tiến hành. Tuy nhiên, dựa trên các phản ứng có hại cho trẻ đang bú mẹ, việc cho con bú cần được ngừng lại và chỉ có thể bắt đầu cho bú lại 4 ngày sau liều điều trị cuối cùng.
- Đối với khả năng sinh sản. Chưa có dữ liệu trên người về ảnh hưởng của thuốc đối với khả năng sinh sản. Các thí nghiệm trên chuột đực và chuột cái ở mức xấp xỉ gấp 2 lần và 6 lần liều khuyến nghị ở người không cho thấy khả năng ảnh hưởng đến sinh sản. Chưa có nghiên cứu ảnh hưởng của thuốc đến tính trùng, cũng như các nguy cơ ảnh hưởng đến tinh trùng sau 3 tháng điều trị bằng thuốc. Tuy nhiên khuyến nghị được đưa ra là nam giới trong độ tuổi sinh sản cần sử dụng biện pháp tránh thai hiệu quả trong thời gian điều trị và sau ít nhất 3 tháng sau liều cuối cùng.
- Chưa có nghiên cứu về ảnh hưởng quá liều của thuốc.
Nhìn chung, dựa trên những phát hiện từ các nghiên cứu về sinh sản ở động vật, Molnupiravir có thể gây hại cho thai nhi khi dùng cho người mang thai. Vì vậy, thuốc không được khuyến cáo sử dụng trong thời kỳ mang thai. Thuốc chỉ được phép kê đơn cho người đang mang thai bởi bác sĩ/chuyên gia y tế sau khi cân nhắc lợi ích của việc điều trị lớn hơn nguy cơ đối với bệnh, và khi kê đơn người bệnh được thông báo về những lợi ích đã biết cũng những rủi ro tiềm ẩn của việc sử dụng thuốc trong thời gian này. Phụ nữ có khả năng sinh sản nên sử dụng một phương pháp ngừa thai hiệu quả và nhất quán trong thời gian điều trị bằng thuốc, và trong bốn ngày sau liều cuối cùng. Nam giới có khả năng sinh sản có quan hệ tình dục với phụ nữ có khả năng sinh sản được khuyến cáo sử dụng phương pháp ngừa thai hiệu quả và nhất quán trong khi điều trị bằng thuốc và ít nhất 3 tháng sau liều cuối cùng.
Vấn đề về lạm dụng thuốc
Molnupiravir là thuốc bắt buộc phải được kê đơn sử dụng. Để đảm bảo an toàn, chỉ sử dụng thuốc để điều trị COVID-19 khi có chỉ định của bác sĩ, và sử dụng đúng liều, cũng như thận trọng quan sát các tác dụng phụ gặp phải trong quá trình điều trị. Nếu gặp phải bất cứ phản ứng phụ nào, cần thông báo cho cơ sở y tế để được hỗ trợ và xử trí kịp thời.
Theo cảnh báo từ FDA, việc mua Molnupiravir không được chỉ định có thể gây các hậu quả nghiêm trọng. Các sản phẩm thuốc không có giấy phép hay mua không rõ nguồn gốc không được đảm bảo chính hãng và an toàn, có thể chứa nhiều hóa chất và các thành phần không được kiểm duyệt. Bên cạnh đó, việc sử dụng Molnupiravir không theo chỉ dẫn gây kém hiệu quả, đồng thời dẫn đến các tác dụng phụ kéo dài và gây hại cho sức khỏe.
Đối với các loại thuốc kháng virus chỉ nên dùng trong vòng 7 ngày sau khi xuất hiện triệu chứng đầu tiên (thường là sốt). Nếu quá 7 ngày mà chỉ số CT khi test RT-PCR vẫn dưới 25 hoặc test nhanh có vạch T đậm thì có thể tham khảo ý kiến bác sĩ trước khi dùng. Mỗi đợt nên dùng 5-7 ngày hoặc theo đúng hướng dẫn của chương trình thử nghiệm. Khi đang dùng thuốc kháng virus, cần cân nhắc rất cẩn thận việc kết hợp với thuốc kháng viêm corticoid, do corticoid ức chế hệ miễn dịch của cơ thể, khiến virus dễ dàng nhân lên hơn.
Hiện Việt Nam có các loại thuốc Favipiravir 200/400mg, Molnupiravir 200/400mg (do Merck nghiên cứu) và Nirmartrelvir/ritonavir (Paxlovid do Pfizer nghiên cứu). Các thuốc khác (đường uống) về cơ bản là không có tác dụng. Molnupiravir là thuốc được cấp phép để điều trị Covid-19 nhẹ và vừa. Thuốc Molnupiravir đang được dùng trong chương trình thử nghiệm, nên không bán công khai mà được phát miễn phí cho các F0 đủ điều kiện và bắt buộc phải tuân thủ nghiêm theo quy trình. Do vậy, việc tự ý mua và sử dụng là trái quy định. Cục Quản lý Dược (Bộ Y tế) khẳng định, việc mua, bán, sử dụng các thuốc không được phép lưu hành trên thị trường là vi phạm nghiêm trọng quy định của Luật dược và tiềm ẩn nguy cơ ảnh hưởng xấu đến sức khỏe người dân, giảm hiệu quả phòng chống dịch, nguy cơ thuốc giả, thuốc nhập lậu.
Nhìn chung, tuyệt đối không tự ý tìm mua và dùng thuốc trị COVID-19 theo mách bảo. Điều này có thể dẫn đến việc lạm dụng, không mang lại lợi ích gì hơn so với không dùng thuốc, mà lại tiềm tàng nhiều nguy cơ tác dụng bất lợi với sức khỏe người dùng, thậm chí có thể làm trầm trọng tình trạng COVID-19 ở người bệnh.
Tài liệu tham khảo:
https://www.sciencedirect.com/science/article/pii/S1871402121003490?via%3Dihub
https://www.nejm.org/doi/full/10.1056/NEJMoa2116044
https://www.sciencedirect.com/science/article/pii/S1871402121003490?via%3Dihub
https://www.sciencedirect.com/science/article/pii/S1871402121003490?via%3Dihub
https://www.sciencedirect.com/science/article/pii/S1871402121003490?via%3Dihub
Tham khảo thêm thông tin tại bài viết: Hậu COVID: triệu chứng và phục hồi
-

Uống nước ép bưởi có giúp giảm huyết áp?
Nước ép bưởi cung cấp nhiều dưỡng chất tốt cho sức khỏe. Thức uống này được đánh giá là có khả năng hỗ trợ giảm huyết áp, tuy nhiên có một số điều cần lưu ý...
-

Vai trò gia đình trong hỗ trợ sức khỏe tâm thần con mùa thi
Mùa thi cử vốn là khoảng thời gian các bạn học sinh phải đối mặt với nhiều lo âu, từ kỳ vọng của cha mẹ đến áp lực tự thân và sự cạnh tranh ở trường lớp. Những lúc căng thẳng như thế này, sự thấu hiểu và chăm sóc từ gia đình chính là "liều thuốc" quý giá nhất giúp các em giữ vững tinh thần. Viện Y học ứng dụng Việt Nam sẽ chia sẻ thông tin giúp phụ huynh kết nối với con nhẹ nhàng hơn, giúp các sĩ tử vượt qua kỳ thi một cách thoải mái và tự tin nhất.
-

5 nhóm thực phẩm quan trọng trong chế độ dinh dưỡng sau tuổi 50
Sau tuổi 50, hệ tiêu hóa và khả năng hấp thụ không còn tốt như thời trẻ. Trong giai đoạn này, chế độ dinh dưỡng sau tuổi 50 đóng vai trò là ‘liều thuốc’ tự nhiên giúp sửa chữa cơ thể và nâng cao chất lượng cuộc sống.
-

Bảo vệ da khỏi tác hại của ánh nắng mặt trời trong mùa hè
Mùa hè đến mang theo những ngày nắng rực rỡ, nhưng cũng tiềm ẩn nguy cơ lớn cho làn da của bạn. Ánh nắng mặt trời, dù cần thiết để tổng hợp vitamin D và mang lại cảm giác ấm áp, lại chứa tia cực tím (UV) có khả năng gây tổn thương da nghiêm trọng nếu không được bảo vệ đúng cách.
-

6 loại trái cây tốt cho thận
Thận đảm nhiệm nhiều chức năng để duy trì sức khỏe như điều hòa lượng nước và loại bỏ chất thải. Nếu không chăm sóc thận đúng cách, chức năng thận có thể bị suy giảm. Tham khảo một số loại trái cây tốt cho thận.
-

11 lợi ích sức khỏe từ vỏ cam
Có lẽ ít người biết rằng vỏ cam rất giàu một số chất dinh dưỡng, bao gồm chất xơ, vitamin C và các hợp chất thực vật như polyphenol rất có lợi cho sức khỏe.
-

Ngủ đúng giờ: Bí mật đơn giản giúp giảm huyết áp hiệu quả
Bạn có biết một thói quen đơn giản, dễ thực hiện vào mỗi đêm lại có thể là "chiến lược vàng" để quản lý huyết áp của mình không? Câu trả lời là: Đi ngủ đều đặn mỗi tối.
-

3 nhóm người nên ăn hoặc uống nước dâu tằm
Dâu tằm là loại quả dân dã nhưng giàu dinh dưỡng, đặc biệt là hàm lượng chất chống oxy hóa dồi dào có lợi cho sức khỏe, nhất là với một số nhóm người cụ thể.










