Báo cáo khoa học: mức độ an toàn và hiệu quả của vaccine Sputnik V của Nga
Ngày 23/3, Bộ Y tế đã phê duyệt có điều kiện vaccine cho nhu cầu cấp bách trong phòng chống dịch COVID-19 đối với vaccine Sputnik V của Nga.
Tại Quyết định số 1654/QĐ-BYT do Thứ trưởng Bộ Y tế Trương Quốc Cường ký ban hành phê duyệt có điều kiện đối với vaccine Gam-COVID-Vac (tên khác là Sputnik V) của Nga cho nhu cầu cấp bách trong phòng, chống dịch COVID-19 theo quy định tại Điều 67 Nghị định số 54/2017/NĐ-CP ngày 8/5/2017 của Chính phủ quy định chi tiết một số điều và biện pháp thi hành Luật dược (Nghị định 54/2017/NĐ-CP). Như vậy đây là vaccine phòng COVID-19 thứ 2 được Việt Nam phê duyệt đến nay. Vậy vaccine Sputnik V có hiệu quả và tính an toàn như thế nào?
Nghiên cứu chứng minh tính an toàn và hiệu quả
Theo bài báo cáo khoa học được đăng tải trên tạp chí The Lancet, Denis Logunov và cộng sự đã báo cáo kết quả tạm thời từ thử nghiệm giai đoạn 3 của vaccine Sputnik V COVID-19. Kết quả thử nghiệm cho thấy tác dụng bảo vệ mạnh mẽ nhất quán trên tất cả các nhóm tuổi tham gia. Còn được gọi với tên Gam-COVID-Vac, vaccine sử dụng phương pháp tiếp cận adenovirus tái tổ hợp dị loại – hạt virus Adeno typ huyết thanh 26 (Ad26) và typ 5 (Ad5) của người tái tổ hợp mang gen mã hóa protein S của SARS-CoV-2. Việc sử dụng hai loại huyết thanh khác nhau, được thực hiện cách nhau 21 ngày nhằm mục đích khắc phục bất kỳ khả năng miễn dịch adenovirus nào đã tồn tại từ trước trong quần thể được tiêm chủng. Trong số các vaccine COVID-19 chính đang được phát triển cho đến nay, chỉ có Gam-COVID-Vac sử dụng phương pháp này; những loại khác, chẳng hạn như vaccine Oxford-AstraZeneca sử dụng cùng một chất liệu cho cả hai liều. Vaccine trước đó cho bệnh do virus Ebola cũng được phát triển tại Trung tâm Nghiên cứu Dịch tễ và Vi sinh Quốc gia Gamaleya (Moscow, Nga) cũng có bản chất tương tự với việc sử dụng virus Ad5 và vesicular stomatitis virus mang mầm bệnh, và nguyên tắc chung với hai vectơ khác nhau đã được sử dụng rộng rãi trong thực nghiệm.
Phương pháp sử dụng adenovirus tái tổ hợp cũng tương tự với vaccine Oxford – AstraZeneca, sử dụng một loại adenovirus của tinh tinh (ChAdOx); vaccine của Johnson & Johnson chỉ sử dụng Ad26 (Dự kiến sẽ sớm có kết quả chi tiết) và vaccine CanSinoBIO – Viện Công nghệ sinh học Bắc Kinh (Ad5) có giai đoạn 3 thử nghiệm bắt đầu vào tháng 9 năm 2020. Các virus mang mầm bệnh được sửa đổi và không thể gây lây nhiễm. Sau đó, chúng xâm nhập vào tế bào và biểu hiện protein đột biến, và dừng lại (vì chúng không thể tiếp tục vòng đời của virus bình thường).
Các tế bào nhiễm vaccine cuối cùng sẽ bị tiêu diệt bởi chính khả năng miễn dịch mà chúng được thiết kế để tạo ra. Các adenovirus tái tổ hợp đã được sử dụng rộng rãi làm vectơ vaccine vì chúng có thể chứa tải lượng di truyền lớn và – và mặc dù không thể tái tạo – nhưng chúng kích hoạt các cảm biến miễn dịch bẩm sinh đủ để đảm bảo sự tham gia mạnh mẽ của hệ thống miễn dịch cơ thể. Do đó, những người được tiêm vaccine không cần thuốc bổ trợ và có thể tạo miễn dịch chỉ sau một liều tiêm duy nhất. Độ bền vật lý của vaccine được cho là có thể cho phép bảo quản ở nhiệt độ khoảng –18°C, mang đến tính khả thi đối với nhiều chuỗi cung ứng. Nhược điểm của vaccine dựa trên adenovirus tái tổ hợp với liều lượng lớn, thường là 1010 hoặc 1011 hạt virus. Do vậy, cần nhu cầu lớn về sản xuất và định lượng cần thiết để triển khai trên quy mô toàn cầu.
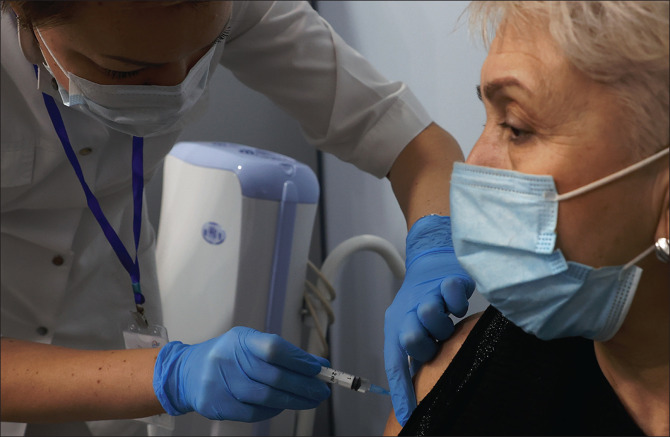
Tính an toàn
Theo dữ liệu vaccine Sputnik V được công bố trong giai đoạn nửa năm trước 2020 (công bố hồi tháng 9 năm 2020) cho thấy, kết quả thử nghiệm vaccine là an toàn và đầy hứa hẹn, mang đến các dấu hiệu đáp ứng miễn dịch ở mức phù hợp với khả năng bảo vệ. Người được tiêm chủng tạo ra các phản ứng kháng thể mạnh mẽ với vaccine, bao gồm các kháng thể trung hòa, tỷ lệ của tổng số globulin miễn dịch ức chế virus liên kết với thụ thể của nó. Các bằng chứng cũng cho thấy phản ứng của tế bào T phù hợp với phản ứng miễn dịch.
Dữ liệu từ báo cáo tạm thời trong giai đoạn 3 trình bày các kết quả cho hơn 20.000 người tham gia, 75% trong được chỉ định tiêm vaccine và theo dõi các phản ứng bất lợi và nhiễm trùng. Đối tượng tham gia từ 18 tuổi trở lên, khoảng 60% là nam và hầu hết đều là người da trắng. Các bệnh đi kèm - một nguy cơ đã biết đối với mức độ nghiêm trọng của COVID-19 – gặp phải ở khoảng ¼ số người tham gia thử nghiệm. Một số chỉ số kết quả khác bao gồm:
- 62 (1-3%) trong số 4902 trường trong nhóm đối chứng và 16 (0-1%) trong số 14.964 đối tượng trong nhóm tiêm vaccine đã xác nhận nhiễm SARS-CoV-2 từ ngày 21 sau khi tiêm liều vaccine đầu tiên.
- Biểu đồ phân tích theo thời gian về tỷ lệ mắc bệnh ở hai nhóm cho thấy khả năng miễn dịch cần thiết để ngăn ngừa bệnh xuất hiện trong vòng 18 ngày kể từ liều tiêm đầu tiên. Sự bảo vệ đó được thất trên tất cả các nhóm tuổi, bao gồm cả những người trên 60 tuổi.
- Các trường hợp được tiêm chủng nhưng đồng thời cũng bị nhiễm bệnh cho thấy mức độ nghiêm trọng của bệnh giảm khi khả năng miễn dịch được phát triển.
- Ba trường hợp tử vong đã xảy ra trong nhóm tiêm vaccine ở những người có nhiều bệnh nền đi kèm, và tử vong được coi là không liên quan đến vaccine.
- Không có tác dụng phụ nghiêm trọng liên quan đến vaccine được ghi nhận, nhưng các tác dụng phụ nghiêm trọng không liên quan đến vaccine đã được báo cáo ở 45 người tham gia trong nhóm được tiêm; và ở 23 người tham gia từ nhóm đối chứng.
- Hiệu quả của vaccine – dựa trên số trường hợp COVID-19 được xác nhận sau 21 ngày sau liều đầu tiên được báo cáo là 91,6% (95% CI 85,6–95,2), và điều này được đề xuất để giảm mức độ nghiêm trọng của bệnh sau một liều tiêm duy nhất, khuyến khích cho các chiến lược tiết kiệm vaccine trong thời điểm hiện tại.
Tham khảo thêm thông tin tại: So sánh bản chất 3 loại vaccine Covid-19 của Pfizer-BioNTech, Moderna và Johnson&Johnson
-

6 lợi ích sức khỏe khi thường xuyên ăn đậu phụ
Là một món ăn bình dân rẻ tiền nhưng đậu phụ lại chứa nguồn dinh dưỡng rất tốt cho sức khỏe. Hãy khám phá những thay đổi tích cực của cơ thể khi chúng ta thường xuyên ăn đậu phụ.
-

10 lợi ích của việc ca hát đối với sức khỏe
Việc cất tiếng hát mang lại nhiều giá trị tích cực cho cả cơ thể và tinh thần. Các bằng chứng khoa học cho thấy ca hát không chỉ là một hình thức giải trí mà còn là một liệu pháp hỗ trợ sức khỏe hiệu quả.
-

Uống nước ép bưởi có giúp giảm huyết áp?
Nước ép bưởi cung cấp nhiều dưỡng chất tốt cho sức khỏe. Thức uống này được đánh giá là có khả năng hỗ trợ giảm huyết áp, tuy nhiên có một số điều cần lưu ý...
-

Vai trò gia đình trong hỗ trợ sức khỏe tâm thần con mùa thi
Mùa thi cử vốn là khoảng thời gian các bạn học sinh phải đối mặt với nhiều lo âu, từ kỳ vọng của cha mẹ đến áp lực tự thân và sự cạnh tranh ở trường lớp. Những lúc căng thẳng như thế này, sự thấu hiểu và chăm sóc từ gia đình chính là "liều thuốc" quý giá nhất giúp các em giữ vững tinh thần. Viện Y học ứng dụng Việt Nam sẽ chia sẻ thông tin giúp phụ huynh kết nối với con nhẹ nhàng hơn, giúp các sĩ tử vượt qua kỳ thi một cách thoải mái và tự tin nhất.
-

5 nhóm thực phẩm quan trọng trong chế độ dinh dưỡng sau tuổi 50
Sau tuổi 50, hệ tiêu hóa và khả năng hấp thụ không còn tốt như thời trẻ. Trong giai đoạn này, chế độ dinh dưỡng sau tuổi 50 đóng vai trò là ‘liều thuốc’ tự nhiên giúp sửa chữa cơ thể và nâng cao chất lượng cuộc sống.
-

Bảo vệ da khỏi tác hại của ánh nắng mặt trời trong mùa hè
Mùa hè đến mang theo những ngày nắng rực rỡ, nhưng cũng tiềm ẩn nguy cơ lớn cho làn da của bạn. Ánh nắng mặt trời, dù cần thiết để tổng hợp vitamin D và mang lại cảm giác ấm áp, lại chứa tia cực tím (UV) có khả năng gây tổn thương da nghiêm trọng nếu không được bảo vệ đúng cách.
-

6 loại trái cây tốt cho thận
Thận đảm nhiệm nhiều chức năng để duy trì sức khỏe như điều hòa lượng nước và loại bỏ chất thải. Nếu không chăm sóc thận đúng cách, chức năng thận có thể bị suy giảm. Tham khảo một số loại trái cây tốt cho thận.
-

11 lợi ích sức khỏe từ vỏ cam
Có lẽ ít người biết rằng vỏ cam rất giàu một số chất dinh dưỡng, bao gồm chất xơ, vitamin C và các hợp chất thực vật như polyphenol rất có lợi cho sức khỏe.