Vaccine VBC-Covid19-154 của Vingroup với mục tiêu góp phần đẩy lùi Covid 19 ở Việt Nam.
ARCT-021, còn được gọi là LUNAR-COV19, là một vắc xin COVID-19 trong quá trình thử nghiệm được phát triển bởi Arcturus Therapeutics. Theo dự kiến đã được công bố, tập đoàn Vingroup sẽ hợp tác với Arturus Therapeutic để sản xuất khoảng 200 triệu liều vaccine theo công nghệ này ở Việt Nam mang tên VBC-COV19-154. Vậy loại vacxin này là gì, được chế tạo thế nào, và các chuyên gia đánh giá về công nghệ chế tạo vaccine này như thế nào?
Về Arturus Therapeutic
Arturus Therapeutic, có trụ sở tại San Diego, là một công ty sản xuất mARN tập trung vào việc phát triển vaccine phòng bệnh truyền nhiễm và bệnh lý cơ hội hiếm gặp về gan và hô hấp. Arturus Therapeutic sở hữu độc quyền các công nghệ như Lunar Lipid-mediated delivery, công nghệ mARN tự sao chép và tự nhân bản mARN và sản xuất cải tiến dược chất về mARN với công thức sản phẩm LUNAR.
Arcturus đang ở giai đoạn nghiên cứu lâm sàng vacxin đông khô mARN phòng covid-19. Công nghệ này cũng đang được ứng dụng bởi 209 công ty trên nhiều lĩnh vực khác nhau và cũng là đối tác của nhiều tổ chức như Duke-National University of Singapore (NUS) Medical School, Pharmaceuticals, Ultragenyx, Takeda, CureVac, Synthetic Genomics, hiệp hội xơ nang…
Về Duke-National University of Singapore (NUS) Medical School
Duke-NUS là trường y khoa đầu vào sau đại học hàng đầu của Singapore, được thành lập vào năm 2005 với sự hợp tác chiến lược, do chính phủ lãnh đạo giữa hai học viện đẳng cấp thế giới: Trường Y Đại học Duke và Đại học Quốc gia Singapore (NUS).
Duke-NUS là trường y khoa hàng đầu của Singapore, được thành lập vào năm 2005 với sự hợp tác chiến lược, do chính phủ lãnh đạo giữa hai học viện đẳng cấp thế giới: Trường Y- Đại học Duke và Đại học Quốc gia Singapore (NUS). Thông qua chương trình giảng dạy sáng tạo, sinh viên tại Duke-NUS được đào tạo, sẵn sàng tham gia vào hệ sinh thái y sinh và chăm sóc sức khỏe ở Singapore. Duke-NUS đã trở nên nổi tiếng quốc tế thông qua các chương trình nghiên cứu đặc trưng. Duke – Nus cũng có quan hệ đối tác chặt chẽ với Dịch vụ Y tế Singapore (SingHealth), tập đoàn chăm sóc sức khỏe lớn nhất Singapore.
Về Vingroup và Công ty CP Công nghệ Sinh học VinBiocare
Vingroup là Tập đoàn kinh tế đa ngành lớn nhất Việt Nam và là một trong những Tập đoàn kinh tế lớn nhất Đông Nam Á. Tập đoàn hoạt động trong 3 lĩnh vực kinh doanh cốt lõi, bao gồm Công nghệ - Công nghiệp - Thương mại Dịch vụ. Vingroup luôn không ngừng sáng tạo, phát triển để kiến tạo hệ sinh thái các sản phẩm dịch vụ đẳng cấp, góp phần đem đến cho thị trường những sản phẩm – dịch vụ theo tiêu chuẩn quốc tế, từ đó góp phần nâng cao chất lượng cuộc sống của người Việt và vị thế của thương hiệu Việt Nam trên trường quốc tế. Về mảng Khoa học sức khoẻ, VinGroup có hệ thống Bệnh viện Vinmex, khoa Y của trường Đại học VinUni…. Và trong thời gian qua VinGroup đã thành lập Công ty CP Công nghệ Sinh học VinBiocare với trọng tâm về vaccine.
Công nghệ mARN tự sao chép và nhân bản mARN (STARR) của Duke – Nus
Vaccine COVID-19 hay còn có tên gọi là ARCT-021 được phát triển bởi trường Y DUKE-NUS, tạo ra phản ứng miễn dịch với protein đột biến của virus SARS-CoV-2. ARCT-021 là loại vacxin đông khô, không có vector virus và chỉ cần một liều duy nhất có khả năng bảo vệ khỏi sự đa dạng của các biến thể virus và có thể sử dụng để tái liều định kỳ. Trong khi những vaccine mARN cần được bảo quản trong môi trường lỏng đông lạnh, thì ARCT-021 là loại vaccine đông khô giúp duy trì hiệu quả trong điều trị trong khi không thể đáp ứng được chuỗi bảo quản cực lạnh, dưới -700 C của những vaccine khác.
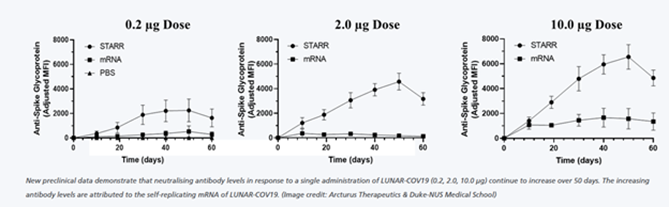
Thử nghiệm lâm sàng LUNAR-COV19 trên người được bắt đầu vào tháng 7 năm 2020 và ngày 4 tháng 1 năm 2021, Arcturus Therapeutics bắt đầu thử nghiệm lâm sàng giai đoạn 2 (pha 2). Dữ liệu tiền lâm sàng chứng minh rằng mức độ kháng thể trung hòa đáp ứng với một liều vaccine LUNAR-COV19 (0,2, 2,0, 10,0 µg) tiếp tục tăng trong 50 ngày. Mức độ kháng thể ngày càng tăng là do mRNA tự sao chép của LUNAR-COV19.
Kết quả thử nghiệm lâm sàng
Theo thỏa thuận, Arcturus sẽ cấp giấy phép độc quyền và Công ty cổ phần Công nghệ sinh học VinBioCare (công ty thành viên của Vingroup) sẽ tiến hành sản xuất vắc xin phòng Covid-19 có tên VBC-COV19-154 được phát triển theo công nghệ tương tự. Công nghệ vaccine mRNA thích hợp để đáp ứng nhanh với các biến thể của virus SARS-CoV-2 nCoVnhờ đặc tính hóa học, vật lý của mRNA vẫn giữ nguyên, ngay cả với những thay đổi trình tự nhỏ cần thiết để phù hợp với các đột biến của virus. Nhờ vậy, việc phát triển vaccine mRNA cho hiệu quả phòng ngừa biến thể của virus SARS-CoV-2 nCoV nhanh chóng và đơn giản, có khả năng chống lại các biến chủng mới nguy hiểm như Alpha, Beta, và cả biến chủng đang rất phổ biến là Delta,... Công nghệ này cũng sử dụng liều vaccine thấp hơn so với vaccine thông thường trong khi kích thích miễn dịch có khả năng sẽ kéo dài hơn, đặc biệt VBC-COV19-154 vận chuyển thuận tiện ở nhiệt độ từ 2 – 8oC, mang đến ưu thế vượt trội về khả năng phổ cập dễ dàng khi triển khai tại cộng cồng và tối ưu chi phí.
Thời gian dự tính Vacxin VCB-COV19-154 sẽ xuất xưởng tại Việt Nam
Theo thoả thuận Arcturus sẽ cấp giấy phép độc quyền và Công ty CP Công nghệ Sinh học VinBioCare (công ty thành viên của VinGroup) sẽ tiến hành sản xuất vaccine phòng COVID-19 có tên VBC-COV19-154 (dựa trên sáng chế vaccine ARCT-154 của Arcturus) đồng thời chuyển giao cho VinBioCare quy trình sản xuất, bao gồm: Bí quyết công nghệ; Đào tạo, chuyển giao, thực hành và kiểm định sản phẩm; cung cấp nguyên liệu đầu vào theo công nghệ độc quyền của Arcturus. Tiến độ chuyển giao dự kiến từ đầu tháng 8 năm 2021. Kết quả thử nghiệm lâm sàng giai đoạn 1 và 2 tại Singapore và Mỹ cho kết quả rất khả quan, tỷ lệ chuyển đổi huyết thanh đạt trên 90%, đạt yêu cầu về độ an toàn và khả năng dung nạp. Số liệu từ trong nghiên cứu pha 1 và pha 2 (0,2, 2,0 µg) trên người trưởng thành chỉ ra rằng liều sử dụng để tăng đáp ứng gắn và trung hòa kháng thể và hoạt hóa tế bào T đặc hiệu có thể chỉ cần một liều duy nhất. Không có biến chứng y khoa nào được ghi nhật. Để đảm bảo an toàn và độ hiệu quả cuả Vaccine trên cộng đồng người Việt, VinBioCare sẽ phối hợp với Cục Khoa học Công nghệ và Đào tạo của Bộ Y Tế Việt Nam đưa vắc xin VCB-COV19-154 vào thử nghiệm lâm sàng giai đoạn 3 tại Việt Nam trên quy mô 20.000 người bao gồm:
+ Giai đoạn 1: thực hiện tại Trường Đại học Y Hà Nội trên 100 người tình nguyện.
+ Giai đoạn 2: thực hiện trên 300 người tình nguyện tại các tổ chức nhận thử và tại cộng đồng ở các tỉnh triển khai nghiên cứu.
+ Giai đoạn 3: số lượng 20.600 đối tượng, tách thành 02 giai đoạn 3a (600 người tình nguyện) và 3b (20.000 người tình nguyện) để sau giai đoạn 3a (kết quả sinh miễn dịch ngày thứ 57) có báo cáo giữa kỳ phục vụ cấp phép khẩn cấp trong trường hợp cần thiết.
Theo kế hoạch, vào tháng 12, 2021, VinBioCare dự kiến sẽ hoàn thiện hồ sơ và gửi Bộ Y tế xin cấp phép khẩn cấp có điều kiện để sử dụng VCB-COV19-154 tại Việt Nam. Dự kiến, lô vaccine đầu tiên sẽ được xuất xưởng vào đầu năm 2022.
Tham khảo thêm thông tin tại bài viết: Nhận biết dị ứng, phản vệ khi tiêm vaccine Covid-19
-

Điều gì xảy ra với huyết áp của bạn khi trời nóng?
Nhiệt độ và huyết áp có mối quan hệ nghịch đảo, nghĩa là khi nhiệt độ tăng, huyết áp sẽ giảm.
-

Công thức sữa chua Hy Lạp với cà phê có lợi nhất cho đường ruột
Việc cho cà phê vào sữa chua là công thức kháng viêm tự nhiên, giàu protein, giàu lợi khuẩn tốt cho đường ruột. Đây là một cách đơn giản bạn có thể áp dụng để chủ động phòng bệnh đường ruột.
-

Phương pháp tự nhiên thúc đẩy tăng trưởng chiều cao cho trẻ trong mùa hè
Việc đẩy mạnh hoạt động thể thao mùa hè cho trẻ em là giải pháp khoa học nhằm thay thế thói quen sử dụng thiết bị điện tử và giảm áp lực học tập. Vận động ngoài trời không chỉ tăng cường sức bền mà còn kích thích hormone tăng trưởng, hỗ trợ phát triển hệ xương khớp tối ưu, đặc biệt là cải thiện chiều cao trong giai đoạn dậy thì.
-

Epigenetic – Đột phá trong chăm sóc sức khỏe cá nhân
Những thành tự nghiên cứu về Bộ gen người vào năm 2003 đã mở ra cánh cửa hiểu biết sâu rộng về di truyền con người. Tuy nhiên, bộ mã DNA không thể giải thích được toàn bộ sự phức tạp về sức khỏe và bệnh tật của từng cá nhân. Di truyền ngoại gen (hay còn gọi là Epigenetic) là một lĩnh vực nghiên cứu các thay đổi trong biểu hiện gen mà không làm thay đổi trình tự DNA. Đây hiện đang là một chủ đề được bàn tán nhiều trong những năm gần đây khi nhu cầu chăm sóc sức khỏe cá nhân ngày càng gia tăng.
-

Tác dụng của nước ép bưởi và 5 lưu ý khi dùng
Nước ép bưởi mang lại nhiều lợi ích như cấp nước, hỗ trợ tiêu hóa và giảm nguy cơ bệnh. Tuy nhiên, loại đồ uống này cũng tiềm ẩn rủi ro, đặc biệt với một số đối tượng cần thận trọng khi sử dụng thường xuyên.
-

3 nhóm người nên ăn hoặc uống nước dâu tằm
Dâu tằm là loại quả dân dã nhưng giàu dinh dưỡng, đặc biệt là hàm lượng chất chống oxy hóa dồi dào có lợi cho sức khỏe, nhất là với một số nhóm người cụ thể.
-

Chế độ ăn keto 6 tuần có thể hỗ trợ cải thiện tình trạng trầm cảm kháng trị
Trầm cảm kháng trị xảy ra khi các triệu chứng của một người không cải thiện sau khi đã thử ít nhất hai loại thuốc chống trầm cảm khác nhau. Một nghiên cứu gần đây đã điều tra tác động của chế độ ăn ketogenic ít carbohydrate đối với người lớn mắc chứng trầm cảm kháng trị.
-

Ánh nắng dư thừa, Vitamin D thiếu hụt: Thực trạng báo động ở trẻ em Việt Nam
Dù sống ở vùng nhiệt đới ngập tràn ánh nắng, tỷ lệ thiếu hụt vitamin D ở trẻ em Việt Nam vẫn đang ở mức báo động. Được ví như "chìa khóa" cho tầm vóc và hệ miễn dịch, việc lãng quên dưỡng chất vàng này đang để lại những hệ lụy sức khỏe kéo dài đến tận tuổi trưởng thành.